1、目的
我们的宗旨是始终为用户提供一定质量水平的抗病毒剂以及抗病毒加工制品。同时为了对社会生活做出贡献、使消费者正确理解这些产品的用法,我们为抗病毒剂和抗病毒加工制品的质量和安全性制定了标准。
2、适用范围
抗病毒剂:适用于在日本或入会规定运用指南附录上登载的国家上市的抗病毒剂。
抗病毒加工制品:适用于在日本或入会规定运用指南附录上登载的国家上市的抗病毒加工制品。
3、抗病毒性能标准
抗病毒剂:将根据抗病毒加工制品的抗病毒活性来确定,未规定作为抗病毒剂的性能标准。 抗病毒加工制品:经过“耐久性试验法”处理后的制品应符合表1所示的抗病毒性能标准。

4、安全性标准
4.1基本事项
抗病毒剂的成分中不能含有以下化学物质。
①未经《化学物质检验法》和《制造法规》(以下简称《化审法》)等有关法律
公布的化学物质。
②第一类特定化学物质;第二类特定化学物质;以及被化审法列为监视化学物质的化学物质。
对于指定为优先评估化学物质的制品,请遵循《自主登录规定》第 3 项第(6) 点中有关质量和安全性数据的规定。
③《原子力基本法》第 20 条规定的放射性物质。
④受《关于限制含有有害物质的家庭用品的法律》及相关法规限制的化学物质。
⑤本会认为存在安全性问题的其他物质
4.2 抗病毒剂的安全性标准
抗病毒剂的安全性试验必须由公共机构或相应的试验机构进行,且必须符合表2中列出的所有安全性标准。
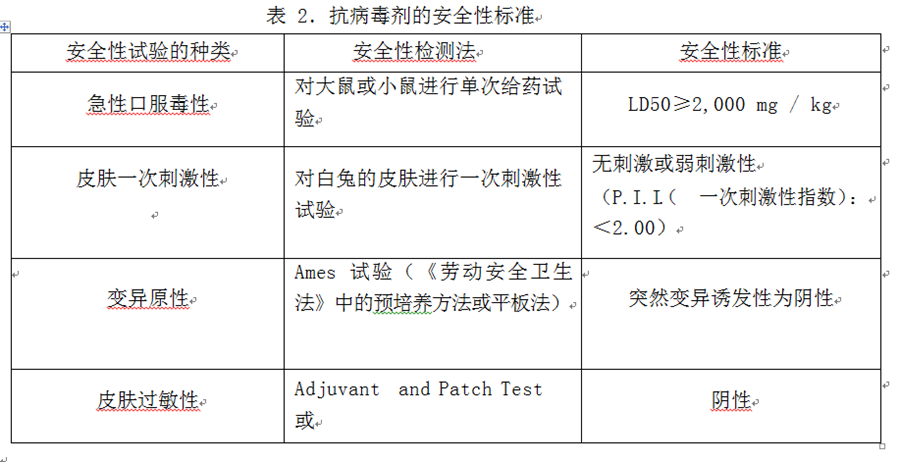
4.3抗病毒加工制品的安全性标准
1)抗病毒加工制品中所含抗病毒剂浓度必须低于已确认安全性的浓度。
若使用稀释原料进行安全性试验,则制品中所含抗病毒剂浓度必须低于已确认安全性的浓度的 1/2。
2)抗病毒加工制品中使用的抗病毒剂必须符合表2所示的安全性标准
5、产品安全数据表(SDS)
抗病毒剂:需提供记载了抗病毒剂的物理化学性能及处理上的注意事项的SDS
抗病毒加工制品:需提供原材料的 SDS